Czy moje dziecko będzie zdrowe cz. 4
Jak często powstają zarodki nieprawidłowe?
Według danych naukowych, ryzyko urodzenia chorego dziecka jest najniższe u kobiet między 26. a 30. rokiem życia. U kobiet w wieku 31 lat, zarodki aneuploidalne (z wadą chromosomową) powstają z częstością 31%. W wieku 35 lat, ryzyko wynosi 34,5%, u kobiet 39-letnich sięga prawie 53%, a u 42-letnich przekracza już 75%. Innymi słowy, szansa na uzyskanie zdrowego zarodka u kobiety w wieku lat 42 to 25%. Więcej szczegółów na wykresie poniżej.
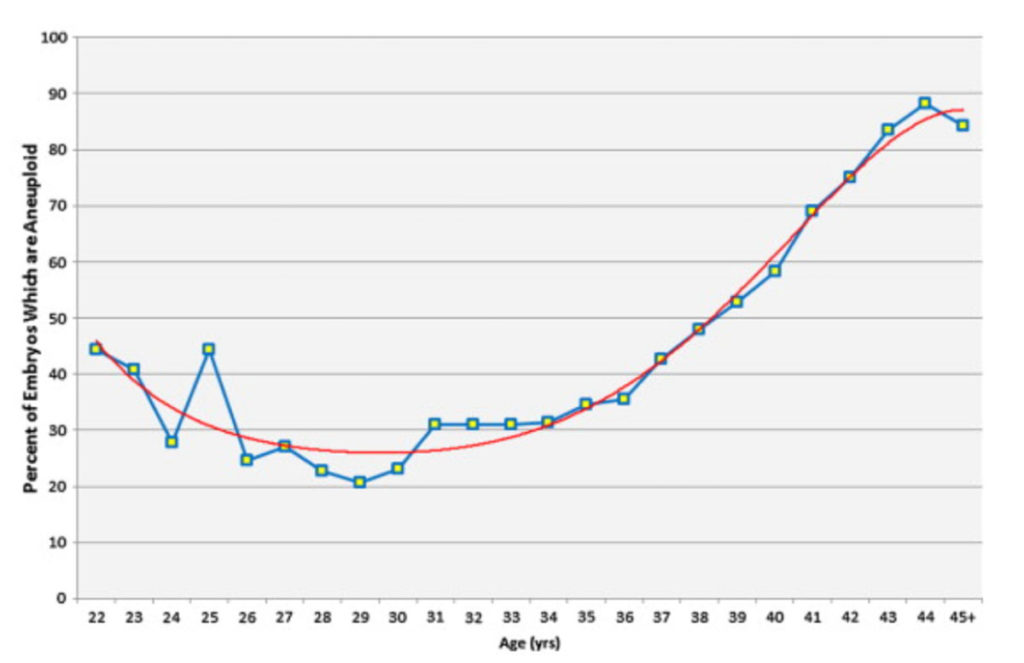
Wykres: Odsetek aneuploidalnych zarodków w zależności od wieku kobiety. Źródło: JM. Franasiak, EJ Forman, KH Hong et al. The nature of aneuploidy with increasing age of the female partner: a review of 15,169 consecutive trophectoderm biopsies evaluated with comprehensive chromosomal screening. Fert Ster 2014: 101(3), p. 656-663.
Jak zastosowanie diagnostyki przedimplantacyjnej zwiększa skuteczność?
Jedną z głównych zalet PGT-A, czyli diagnostyki zarodków pod kątem aneuploidii (wad chromosomowych) jest wyższa skuteczność zabiegu in vitro – większy wskaźnik implantacji, ciąż klinicznych oraz żywych urodzeń u kobiet po 35. roku życia:
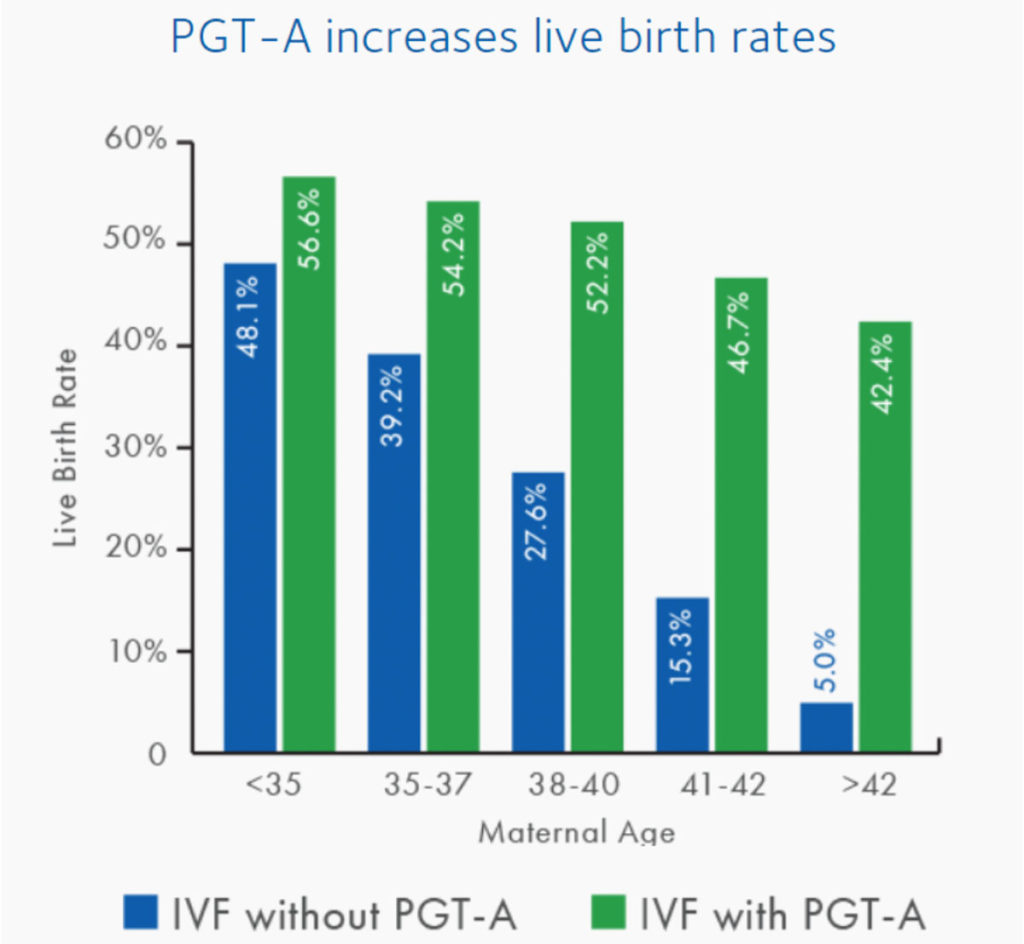
Wykres: Odsetek żywych urodzeń w zależności od wieku kobiety, przy zastosowaniu (zielone słupki) i bez zastosowania (niebieskie słupki) diagnostyki przedimplantacyjnej zarodków. Źródło: PGT-A | Embryo Chromosomal Abnormalities Test | CooperSurgical Fertility | CooperSurgical Fertility Companies
W poprzednim artykule (część 3) wspomniałam także o zmniejszonym wskaźniku poronień u kobiet po 35. roku życia.
Diagnostyka genetyczna zarodków to zatem krok milowy w stronę zmniejszenia ryzyka poronień i powikłań położniczych oraz zwiększenia szans na urodzenie zdrowego dziecka, pomimo zaawansowanego wieku kobiety.
Mozaicyzm
Wspominałam już o nim w 3. części cyklu artykułów dotyczących PGT, jednak chciałabym skupić się na tym, czy i kiedy warto takie zarodki transferować.
Istnieją różne rodzaje zarodków mozaikowych. Jeśli między 20 a 80% komórek pobranych w czasie biopsji trofektodermy ma nieprawidłowy status chromosomowy, zarodek uznawany jest za mozaikę, a odsetek aneuploidalnych komórek podawany jest zazwyczaj na wyniku. Aneuploidia może dotyczyć jednego, dwóch, a także większej ilości chromosomów (wtedy mówimy o złożonych zaburzeniach chromosomowych).
Mozaicyzm jest pułapką diagnostyczną, bo istnieje ryzyko, że pobrany fragment trofektodermy (z której rozwija się łożysko) nie będzie odzwierciedlał faktycznego statusu genetycznego węzła zarodkowego (z którego rozwija się płód). Nie udowodniono jak dotąd, że zarodek „wyrzuca” nieprawidłowe komórki do trofektodermy, choć niektóre publikacje potwierdzają, że taki mechanizm samonaprawy może istnieć. Zatem jest ryzyko, że zarodek z prawidłowym węzłem zarodkowym, a nieprawidłową trofektodermą, uznamy za aneuploidalny. I odwrotnie – że zarodek z wadami genetycznymi uznamy na podstawie pobranych, euploidalnych komórek, za prawidłowy. Takie ryzyko jest bardzo niskie, jednak istnieje, a więc nigdy diagnostyka przedimplantacyjna nie będzie rozpatrywana w kategoriach stuprocentowej skuteczności.
Podobne zjawisko, które polega na innym kariotypie łożyska, a innym płodu, można zaobserwować w czasie ciąży. Jest to tzw. confined placental mosaicism, dotyczy ok. 1-2% ciąż i może powodować problemy diagnostyczne w czasie badania prenatalnego polegającego na biopsji kosmówki. To taka biopsja trofektodermy w skali makro, już w trakcie ciąży. Jak widzimy, wówczas mozaicyzm jest bardzo rzadki, co oznacza, że większość wad obserwowanych na etapie blastocysty, może ulegać samonaprawie.
Co zrobić, jeśli zarodek uznano za mozaikę?
Odpowiedzi poszukajmy znowu w rzetelnych źródłach naukowych. Zacznijmy od publikacji z 2019 roku: zarodki z mozaicyzmem mogą być transferowane, jeśli nie ma dostępnych zarodków euploidalnych (prawidłowych), a skuteczność tych transferów przedstawia poniższy wykres.
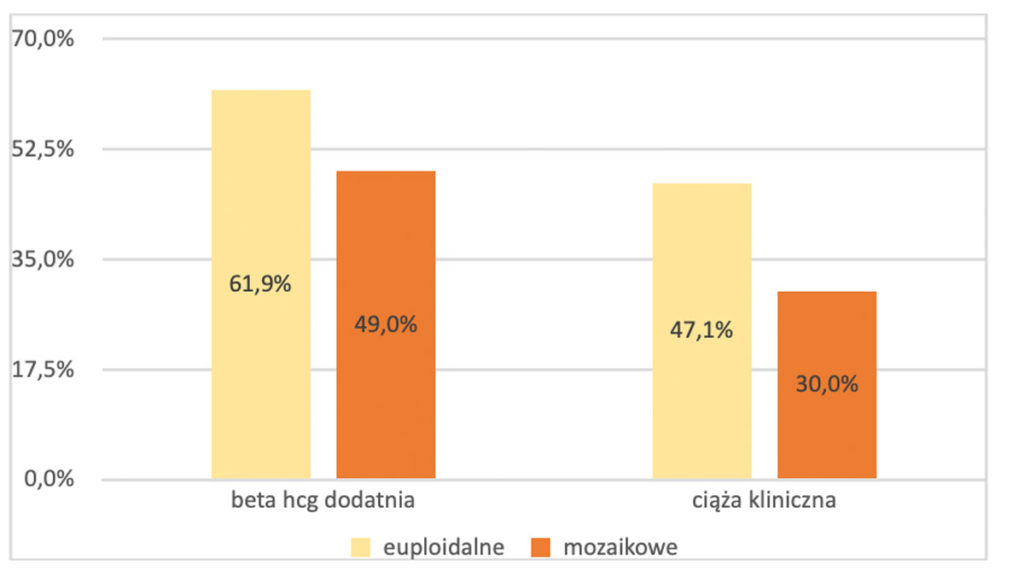
Wykres: Skuteczność transferów zarodków z prawidłowym statusem chromosomowym (euploidalnych) oraz mozaikowych. Źródło: AR Victor, JC Tyndall, AJ Brake et al. One hundred mosaic embryos transferred prospectively in a single clinic: exploring when and why they result in healthy pregnancies. Fert Ster 2019:111(2), p. 280-293.
W nowszej publikacji, z grudnia 2021 roku wykazano, że zarodki z mozaicyzmem średniego (30-50% komórek aneuploidalnych) i niskiego (20-30% komórek aneuploidalnych) stopnia mogą posiadać taki sam potencjał rozwojowy, jak te zupełnie zdrowe.
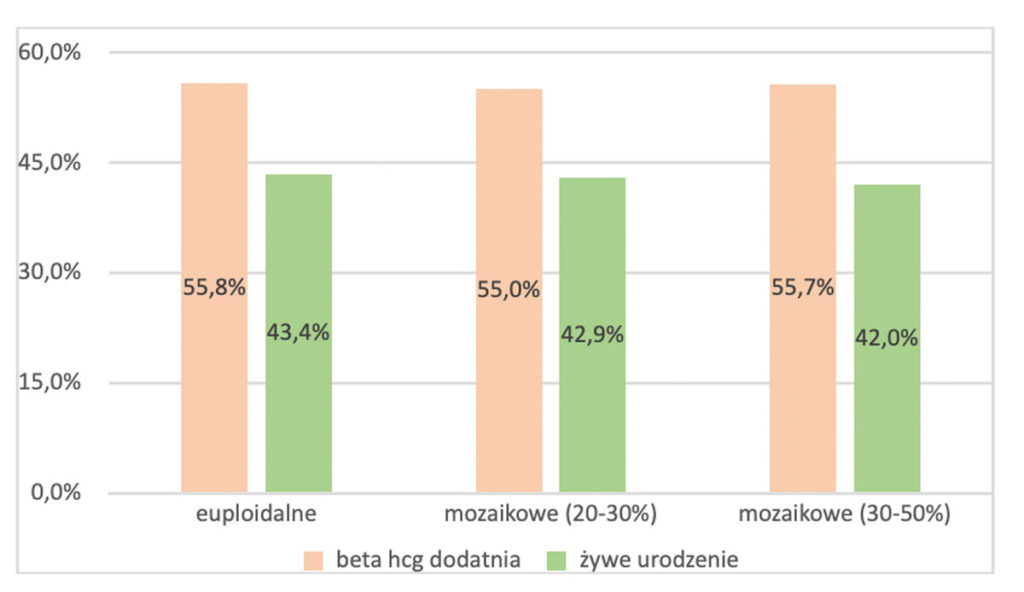
Wykres: Skuteczność transferów zarodków z prawidłowym wynikiem PGT-A (euploidalnych) oraz zarodków mozaikowych ze średnim i niskim odsetkiem komórek aneuploidalnych. Źródło: A. Capalbo, M.Poli, L. Rienzi et al. Mosaic human preimplantation embryos and their developmental potential in a prospective, non-selection clinical trial. AJHG 2021:108, p. 2238-2247.
Wiemy już, że możliwy jest transfer niektórych zarodków mozaikowych, jednak poza stopniem mozaicyzmu, istnieją także ograniczenia dotyczące chromosomów objętych zaburzeniami:

Tabela: Ustalanie priorytetu zarodków do transferu w przypadku wad chromosomowych. Źródło: FR Grati, G Gallazzi, L Branca et al. An evidence-based scoring system for prioritizing mosaic aneuploid embryos following preimplantation genetic screening. Reprod Biomed Online 2018:36, p. 442-449.
W tabeli wykazano mutacje dotyczące zwielokrotnienia liczby chromosomów (trisomie), jednak ten sam system ustalania priorytetów do transferu może być zastosowany w przypadku monosomii, ze względu na podobne ryzyko.
Każda decyzja dotycząca przeniesienia do macicy zarodka mozaikowego, musi zostać poprzedzona konsultacją z lekarzem genetykiem. W czasie takiej konsultacji pacjenci powinni zostać poinformowani o ryzyku.
Co wpływa na skuteczność diagnostyki przedimplantacyjnej?
1. Biopsja trofektodermy
Wspominałam już o tym, że biopsja jest zabiegiem inwazyjnym i może spowodować uszkodzenie, a nawet degenerację zarodka, choć ryzyko jest bardzo niewielkie. Biopsja zarodków ze słabej jakości trofektodermą (niewiele, luźno połączonych komórek) powinna zostać przedyskutowana z embriologiem.
2. Rebiopsja
W przypadku, jeśli wynik badania genetycznego nie może zostać wydany w sposób wiarygodny (niewielka ilość dostępnego materiału do badania, degradacja materiału, niepowodzenie amplifikacji, zanieczyszczenie materiału, mozaicyzm), konieczna jest ponowna biopsja trofektodermy. Zarodek jest rozmrażany, embriolog pobiera próbkę materiału i mrozi zarodek ponownie. Taki zabieg jest związany z podwyższonym ryzykiem, przede wszystkim ze względu na dużą ilość manipulacji na zarodku oraz większą ilość pobranych komórek. W jednym z badań naukowych wykazano, że na biopsji większej ilości materiału mogą ucierpieć głównie słabej jakości zarodki:
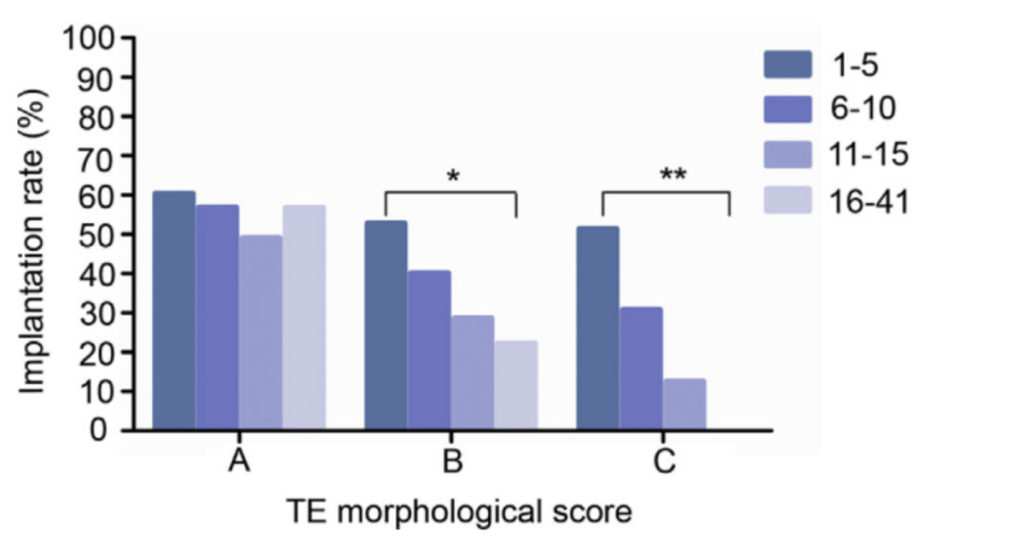
Wykres: Wpływ biopsji różnej ilości komórek trofektodermy na wskaźnik implantacji zarodków, w zależności od jakości trofektodermy (A-dobra jakość, B – średnia jakość, C – słaba jakość). Źródło: S Zhang, K Luo, D Cheng et al. Number of biopsied trophectoderm cells is likely to affect the implantation potential of blastocysts with poor trophectoderm quality. Fert Ster 2016: 105(5), p. 1222-1227.
Jednak jak wynika z wykresu poniżej, już biopsja około 10 komórek może ograniczyć szanse na implantację oraz ciążę kliniczną. Pomimo, że biopsja na etapie zarodka blastomerowego (w dniu 3. rozwoju) jest dużo bardziej niebezpieczna dla dalszych podziałów i formowania zarodka, także biopsja w stadium blastocysty nie jest zupełnie obojętna. Należy mieć to na uwadze szczególnie, w przypadku zarodków słabej jakości oraz tych, które podlegają rebiopsji.
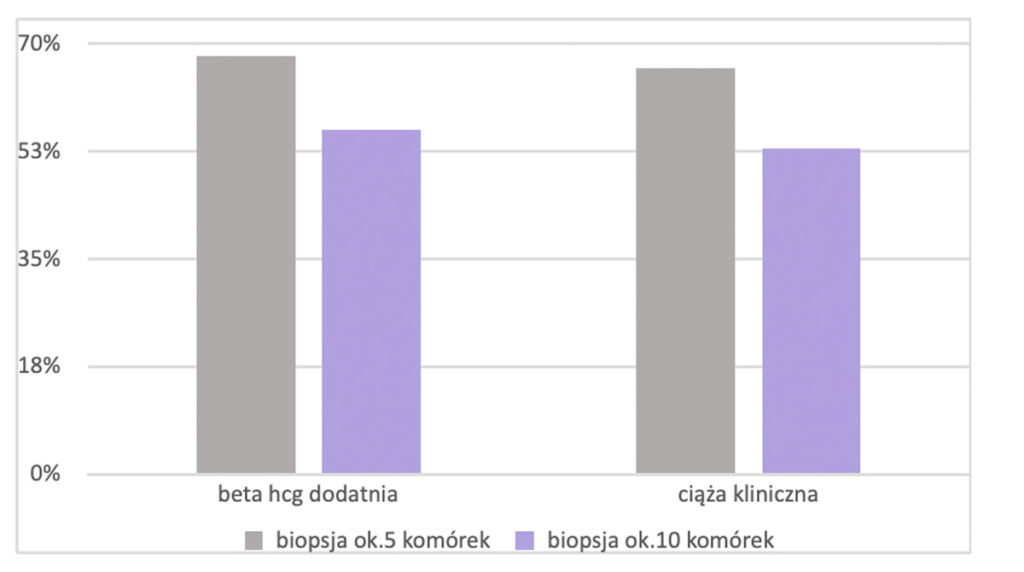
Wykres: Skuteczność transferu zarodków po biopsji trofektodermy, w zależności od ilości pobranych komórek. Źródło: L Guzman, D Nunez, R Lopez et.al. The number of biopsied trophectoderm cells may affect pregnancy outcomes. Journal of Assisted Reproduction and Genetics. 2019:36; p. 145-151.
3. Biopsja trofektodermy na zarodkach zamrożonych
Istnieje możliwość wykonania badania genetycznego na zarodkach, które już zostały zamrożone. Dzieje się tak na przykład, gdy pacjenci otrzymują nieprawidłowe wyniki badań genetycznych już po powstaniu zarodków lub w przypadku poronienia, gdy wykryto wadę genetyczną w materiale poronnym. Wówczas zarodki są rozmrażane, embriolog pobiera materiał do badania i ponownie mrozi zarodki. Taka procedura może być przeprowadzona z powodzeniem, nie skutkuje to ograniczeniem szans zarodka, a wyłączne ryzyko wiąże się z podwójnym mrożeniem zarodka. Witryfikacja (proces mrożenia) ma jednak wysoką skuteczność i ewentualne ryzyko, że zarodek nie przetrwa dwóch serii mrożenia/rozmrażania jest bardzo niskie (ok. 2%). Większy problem może wystąpić dopiero wówczas, gdy wynik badania genetycznego będzie niediagnostyczny i wówczas konieczna będzie rebiopsja (patrz punkt 2.).
Co dzieje się z zarodkami, których wynik badania genetycznego jest nieprawidłowy lub niediagnostyczny?
Zarodki takie trafiają do banku komórek rozrodczych i zarodków i są przechowywane na koszt klinik.
Zarodka, który jest obarczony wadą genetyczną, nie można transferować, ze względu na ryzyko poronienia i ewentualnych jego powikłań oraz urodzenia dziecka chorego.
Zarodek niediagnostyczny może zostać transferowany za pisemną zgodą pacjentów, ponieważ nieznany jest jego status genetyczny. Inną możliwością jest jego ponowne poddanie diagnostyce przedimplantacyjnej (ponowna biopsja komórek zarodka i wysłanie materiału do badania). Zazwyczaj rebiopsja i powtórne badanie zarodków niediagnostycznych są wykonywane bezpłatnie.
Dowiedz się więcej czytając nasze artykuły







