Czy moje dziecko będzie zdrowe, czyli jak badamy zarodki? część 1
To jedno z pytań, które słyszę prawie zawsze rozmawiając z pacjentami przed transferem, a powinno ono paść dużo, dużo wcześniej.
Standardowo zarodki podlegają ocenie morfologicznej (ocenie budowy zarodków). Embriolog ocenia między innymi ich budowę, ilość komórek, obecność fragmentacji oraz inne elementy oceny możliwe do wykonania na tym podstawowym etapie. Znacznie lepszą ocenę zarodków otrzymuje się w przypadku prowadzenia hodowli zarodków w specjalistycznym inkubatorze z systemem Time-Lapse. W porównaniu z klasycznym sposobem obserwacji, ocena kluczowych etapów rozwoju zarodka jest bardziej precyzyjna. Dzięki temu systemowi embriolog może dodatkowo wykryć nieprawidłowości. Może zauważyć obecność multinukleacji w zarodku (czyli pojawianie się większej liczby jąder w obrębie jednej komórki zarodkowej), zobaczyć, jak przebiegają podziały komórkowe, ocenić procesy morfokinetyczne i sprawdza prawidłowy przebieg rozwoju na każdym etapie
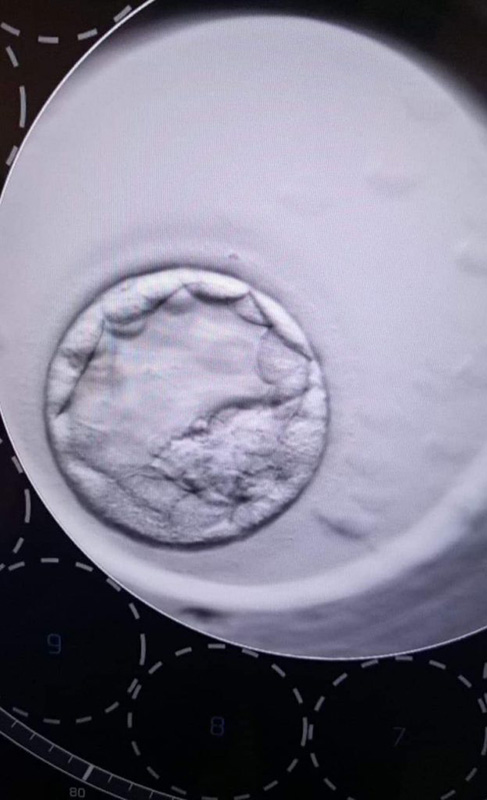
Podgląd w systemie time lapse umożliwia embriologowi ciągłą obserwację podziałów i rozwoju zarodka.
Wciąż jednak nie wiemy, czy zarodek prawidłowy pod względem genetycznym. Aby stwierdzić obecność wady genetycznej (takiej jak np. zespołu Downa, Edwardsa, Patau, Turnera, Klinefeltera czy innych) lub innych mutacji, konieczne jest przeprowadzenie tzw. diagnostyki przedimplantacyjnej – Preimplantation Genetic Testing PGT. Polega ona na zbadaniu materiału genetycznego każdego zarodka z osobna. Standardowo nie wykonuje się tego na żadnym z zarodków. Zatem podając zarodek w czasie transferu, jeśli nie przeprowadzimy szczegółowej diagnostyki przedimplantacyjnej, nie wiemy, czy jest prawidłowy genetycznie i czy będzie się dalej prawidłowo rozwijał.
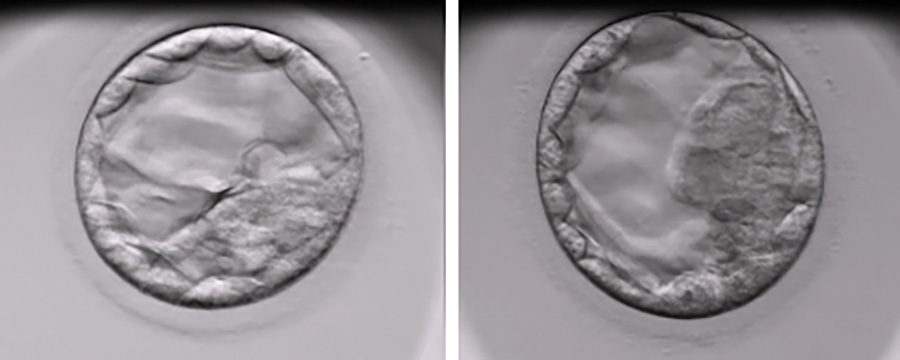
Zarodki: po prawej prawidłowy, a po lewej z wadą genetyczną. Niestety, nieprawidłowości genetyczne nie są widoczne na tym etapie rozwoju.
Spójrzcie sami na zdjęcia – zarodek po prawej stronie jest prawidłowy, a po lewej posiada wadę genetyczną. Wiemy to, ponieważ zarodki zostały zbadane za pomocą PGT. Nie da się tego zweryfikować na podstawie oceny morfologicznej czy dokonując oceny z wykorzystaniem systemu Time-Lapse (na podstawie samych zdjęć i obserwacji zarodka, nie możemy stwierdzić żadnych różnic między nimi. Ich budowa zewnętrzna, ilość komórek i stadium rozwoju są bardzo podobne). To zupełnie inaczej, niż u dorosłych – wystarczy, że spojrzymy na przykład na kogoś z Zespołem Downa i od razu widzimy charakterystyczne cechy budowy twarzy i ciała, które różnią go od kogoś bez tego zespołu. Niestety, na etapie blastocysty, czyli kiedy zarodek ma zaledwie 5 dni, nie da się zobaczyć takich typowych oznak jakiejś wady genetycznej.
Jak w takim razie zbadać zarodki, aby dowiedzieć się, czy są prawidłowe genetycznie i czym jest diagnostyka przedimplantacyjna? Postaram się wyjaśnić Wam poniżej.
Diagnostyka przedimplantacyjna – co to takiego?
Diagnostyka preimplantacyjna pozwala na zminimalizowanie ryzyka przeniesienia chorób genetycznych na dziecko, jeszcze przed zajściem kobiety w ciążę. Metoda ta polega na wykryciu nieprawidłowości DNA zarodka – przed podaniem go do macicy. Wielu parom będącym w grupie ryzyka lub z obciążonym wywiadem genetycznym daje ona szansę na posiadanie zdrowego dziecka.
Celem diagnostyki preimplantacyjnej jest zwiększenie szansy na to, że zarodki, które implantują się w macicy kobiety i z których następnie powstanie ciąża, wolne będą od obciążeń genetycznych, w kierunku których były badane. Zarodki obciążone chorobą uwarunkowaną genetycznie, identyfikowane są na bardzo wczesnym etapie rozwoju tak, aby można było uniknąć ich przeniesienia do macicy i w ten sposób zmniejszyć ryzyko urodzenia dziecka obciążonego poważną chorobą genetyczną. Warto podkreślić, że diagnostyka przedimplantacyjna nie wyklucza wady genetycznej całkowicie.
Terminologia
Istnieje wiele skrótów i określeń diagnostyki przedimplantacyjnej.
PGT – Preimplantation Genetic Testing to najnowsze określenie diagnostyki przedimplantacyjnej, które w ostatnim czasie zostało zaakceptowane przez międzynarodowe stowarzyszenia medyczne zajmujące się zdrowiem reprodukcyjnym (ICMART, ASRM, ESHRE). Zmiany miały na celu znormalizowanie i ujednolicenie terminologii na całym świecie. Wyróżniamy zatem rodzaje PGT:
PGT-A – Preimplantation Genetic Testing for Aneuploidies (dawniej PGS – Preimplantation Genetic Screening) – to diagnostyka dużych wad chromosomowych np. zespołu Downa, Edwardsa, Patau, Turnera i Klinefeltera oraz innych – w których występuje nadmiar lub brak któregoś z chromosomów.
PGT-M – Preimplantation Genetic Testing for Monogenic/Single Gene Defects (dawniej PGD – Preimplantation Genetic Diagnosis) – to diagnostyka niewielkich, pojedynczych mutacji genetycznych na poszczególnych chromosomach, jednak w tym przypadku musimy wiedzieć, czego konkretnie szukamy. Przykładowo, jeśli któreś z rodziców jest obciążone stwierdzoną wadą genetyczną lub jest nosicielem jakiejś mutacji, dokładnie tej samej mutacji szukamy w zarodku. Przykładem może być choroba Huntingtona lub mukowiscydoza.
PGT-SR – Preimplantation Genetic Testing for Structural Rearrangements (również dawnie PGD) – to diagnostyka rearanżacji chromosomowych, czyli wad polegających na przykład na przeniesieniu fragmentu chromosomu na inny chromosom albo utraty fragmentu chromosomu.
Wskazania do wykonania diagnostyki przedimplantacyjnej
Do testu przesiewowego PGT-A, czyli wykluczenia obecności dużych wad chromosomowych:
- wiek matki powyżej 35 lat; (częstość zaburzeń liczbowych chromosomów zwiększa się wraz z wiekiem kobiety starającej się o ciążę, a znaczący wzrost dotyczy już kobiet powyżej 35 roku życia),
- nawracające poronienia samoistne,
- nieudane próby zapłodnienia pozaustrojowego (mimo transferu dobrej jakości zarodków brak implantacji zarodka stwierdzany w USG jako brak ciąży w więcej niż 5 tygodniu po embriotransferze).
Do testów PGT-M/PGT-SR, gdzie szukamy mniejszych wad genetycznych:
- istnienie wysokiego ryzyka przeniesienia choroby genetycznej na potomstwo w przypadku par obciążonych genetycznie (zdiagnozowane nosicielstwo chorób genetycznych);
- diagnostyka mutacji patogennych potwierdzonych u jednego lub obojga rodziców w przypadku obecności choroby genetycznej;
- diagnozowana mutacja jest przyczyną powstania poważnych nieprawidłowości, które mogą pojawić się przed urodzeniem, w czasie dzieciństwa lub w wieku dorosłym;
- istnienie ryzyka choroby genetycznej dziedziczącej się w sposób sprzężony z płcią, jeżeli taki sposób dziedziczenia ustalono na podstawie historii choroby i wywiadu rodzinnego w jej kierunku;
- typowanie HLA (genów układu zgodności tkankowej) dla rodzeństwa wymagającego terapii komórkami macierzystymi;
- potwierdzone nosicielstwo translokacji/inwersji chromosomowej u rodziców.
Nie jest wskazaniem do wykonania diagnostyki przedimplantacyjnej selekcja płci zarodka.
Diagnostyka PGT w celu wyboru płci zarodka jest możliwa tylko w przypadku obecności lub nosicielstwa choroby genetycznej sprzężonej z chromosomem X. W Polsce nie przeprowadza się selekcji płci zarodków bez udokumentowanych wskazań medycznych – wyników badań genetycznych osób chorych oraz pary poddającej się leczeniu.
Przed wykonaniem diagnostyki przedimplantacyjnej zarodków, należy wcześniej spełnić poniższe warunki (są to wymagania określone Ustawą o leczeniu niepłodności z 2015 roku):
- Wykonanie badania kariotypu z limfocytów krwi obwodowej u obojga partnerów. Wynik uzyskacie po ok. 4-6 tygodniach!
- Konsultacja genetyczna – jej celem jest możliwie precyzyjne określenie ryzyka genetycznego dla danej pary i dostosowanie metody badania do tego ryzyka (tak aby je wyeliminować lub zminimalizować).
- Wskazana jest również konsultacja psychologiczna w związku ze złożonością problemu i emocjami, jakie towarzyszyć mogą podejmowaniu ważnych decyzji związanych z diagnostyką preimplantacyjną
- Czasami w przypadku niektórych chorób, konieczne może być również przebadanie członków rodziny, w celu przygotowania do diagnostyki
Decyzję o diagnostyce przedimplantacyjnej należy skonsultować z lekarzem minimum 3 miesiące przed kwalifikacją do zabiegu in vitro. Wynika to z faktu, że laboratorium musi być przygotowane na przeprowadzenie badania genetycznego. Dla niektórych pacjentów konieczne jest zaprojektowanie specjalnych sond DNA pod kątem konkretnej mutacji genetycznej, a to wymaga czasu. Podobnie badania kariotypów, skonsultowanie wyników z genetykiem – to także nie jest kwestia kilku dni.
Tekst opracowany przez starszego embriologa klinicznego Centrum Leczenia Niepłodności Parens Anetę Macur.
Dowiedz się więcej czytając nasze artykuły






